
Salomon Lab - LIght Matters
Plasmonics, hybrid materials for renewable energy, light matter interaction, aerogels, metallic nanostructures, SHG, surface chemistry, photochemistry
Current research at the Salomon lab is focused on interactions between molecules and light at the nanoscale, and real-time imaging of electrode surfaces as part of INREP
.jpg)
איך אפשר לקטוף לחם מאוויר?
חנקן, פחמן, מימן וחמצן, הם יסודות שחיוניים להישרדותו של כל יצור חי.
הצמחים מייצרים מהם מולקולות אורגניות, שמהן אנחנו עשויים, לאחר שאנחנו צורכים את הצמחים או החיות שאוכלות אותם במסגרת שרשרת המזון. בקיצור, בלי היסודות האלה אין חיים. את הפחמן החמצן והמימן הצמחים 'מבשלים' לנו מפחמן דו חמצני בתהליך הפוטוסינטזה ואז כולנו צורכים אותם, בני אדם ,וחיות. אבל מה עם החנקן?
לכאורה, אין דבר זול יותר מחנקן. כל אחד יכול לתפוס איזה ליטר של אוויר- ויהיו ברשותו 780 מ"ל של חנקן - חינם אין כאסף.
בפועל, חנקן שאינו בצורת N2, הוא דווקא די יקר. הקשר המאד-מאד חזק של החנקנים בחנקן שבאוויר, קשר קוולנטי משולש, לא מאפשר לצמחים לפרק את החנקן ולחבר אותו לאטומים אחרים. הם צריכים 'לבנות' על חיידקים ואצות מיוחדות שיפרקו חומר אורגני רקוב קיים ומייצרים חנקות- חנקן חמצני, או לחילופין לחכות לברקים חשמלים שישברו את הקשר החנקני בזמן סערות. זהו הדשן שממנו הם חיים. מכות ברק ומיקרואורגניזמים מפרקי חנקן אין הרבה - אבל בני אדם שרוצים לאכול צמחים או חיות ולקבל מהם חנקן- יש מיליארדים. מי מספק לבני אדם את כל החנקן הזה? במשך אלפי שנים בני אדם פשוט השתמשו בדשן שעשוי מהאורגניזמים שמתו בעבר ועברו פירוק, וגמרו את מאגרי החנקן בקרקע. כאשר נגמר הדשן באירופה, נאלצו לייבא אותו מדרום אמריקה- וכן הלאה. כמות האנשים גדלה עוד ועוד ,אבל כמות החנקן למרבה הצער לא. הוא נשאר באוויר. התוצאה הייתה שמדענים בתחילת המאה ה20 צפו רעב גדול שיכול להביא לסופה של האנושות.
ואז, בדיוק בזמן מלחמת העולם הראשונה הגיע פריץ האבר, כימאי יהודי גרמני עם תושיה: האיש שקטף לחם מהאוויר. על מנת להגיב N2 ו H2 - שני חומרים שקל למצוא אבל קשה להגיב ,מדענים ניסו לפניו לחמם או לחשמל את הגזים בשביל לפרק ולהגיב אותם, אך התוצאות היו מוגבלות. התגובה היא אקסותרמית- כלומר פולטת חום ואינה 'אוהבת חום', אז המשמעות היא שהחום שצריך בשביל לפרק את החנקן, גורם, למרבה הצער, לחנקן ולמימן 'לברוח' זה מזה.
פריץ היקר הביא שני רעיונות חדשניים לתמונה: 1. זרז מתכתי, חומר שלישי, מתווך, שלא מגיב אבל גורם לשני חומרים אחרים להתקרב זה לזה ולהגיב, במקרה הזה הוא חשב על מתכת בשם אוסמיום שאילצה את המימן והחנקן 'לערוך היכרות'. 2. לחץ גבוה: ככה אפשר לגרום לחומר להתפרק בלי לחזור אחורה לגזים המקוריים.
ממשיכו, כימאי בשם בוש, כבר החליף את האוסמיום היקר בברזל הזול והזמין, ואת גז המימן במים כמקור מימן. ככה הצליחו שני הכימאים להכניס בצד אחד אוויר ומים, ולצאת בצד השני עם אמוניה, חומר שממנו קל להכין דשן חנקני ולהאכיל מיליארדי צמחים מפונקים ובני אדם מפונקים אף יותר. מהאמוניה אפשר גם להכין חנקות שמחמצנות במהירות מסחררת חומרים פחממניים לגז, או במלים אחרות להכין פצצות. יחד, שני אלו שינו את העולם , לטוב או לרע... פרס הנובל הגיע במהרה, וגם ייסורי המצפון.
עם קצת סיוע מתכתי אפשר גם לייצר מהחנקות חומר צילום, ננוחלקיקים, ועוד הרבה מאד דברים אחרים. אז תנסו לתפוס קצת חנקן אם אתם יכולים ,זה דורש רק לסגור בקבוק ריק. ואם נתקעתם אחרי זה- תתקשרו לכימאי...
איך זה קשור למעבדה שלנו?
אצלנו עושים פוטוסינתזה מלאכותית - artificial photosynthesis
כלומר מנסים לתעל את האור לריאקציות כימיות- כדי לייצר דלק מאור.



מה הקשר בין דגני בוקר לחומרי הדברה?
חומרי הדברה הינם כימיקלים שתפקידם להגן על גידולים חקלאיים ממזיקים כמו: צמחיה, חרקים, מכרסמים, בקטריות, פטריות וכו'. כאשר מטוסים, כלי עבודה חקלאיים, וחקלאים עצמם מרססים את השדות, חלק מחומרים אלו נשאר ואינו מתנקז עם הגשם או הרוח. לכן, בסופו של דבר עלולים כימיקלים אלו להגיע לצלחת שלנו, בין אם מדובר בירקות,פירות ואף דגני בוקר העשויים משיבולת שועל או תבואה אחרת. החומרים עצמם מסוכנים בחשיפה ארוכה (תלוי בריכוז ובכמות) ועלולים להוביל לתחלואה. בנוסף, היום ידוע שמעל 75% מאפליקציית הריסוס אינן מגיעות ליעדן - מה שגורם לאיבוד עצום בחומרי ההדברה, בעלויות הריסוס, שעות עבודה ומשאבים יקרים שיורדים לטמיון. בעיה נוספת היא נידוף אותו רחף של כימיקלים לחלקות "רגישות" של החקלא המרסס (או לחלקות של חקלאי שכן), הגורם להרס היבול בצורה מוחלטת, או לחילופין לאי-יכולת לשווק את התבואה עקב הצטברות של חומרי הדברה עליהם. הסיבה לכך היא עקב פרמטרים חשובים עליהם המרססים והחקלאים מסתכלים פחות, והם המטאורולוגיה המקומית, והשפעתה על חומרי ההדברה ו"תזוזתם" באוויר. לדוגמא: שינוי קטן במהירות הרוח יכול להוביל לאחוזי "איבוד" ניכרים, כמו כן גם טמפ' גבוהות (התנדפות החומרים) וכן הלאה.
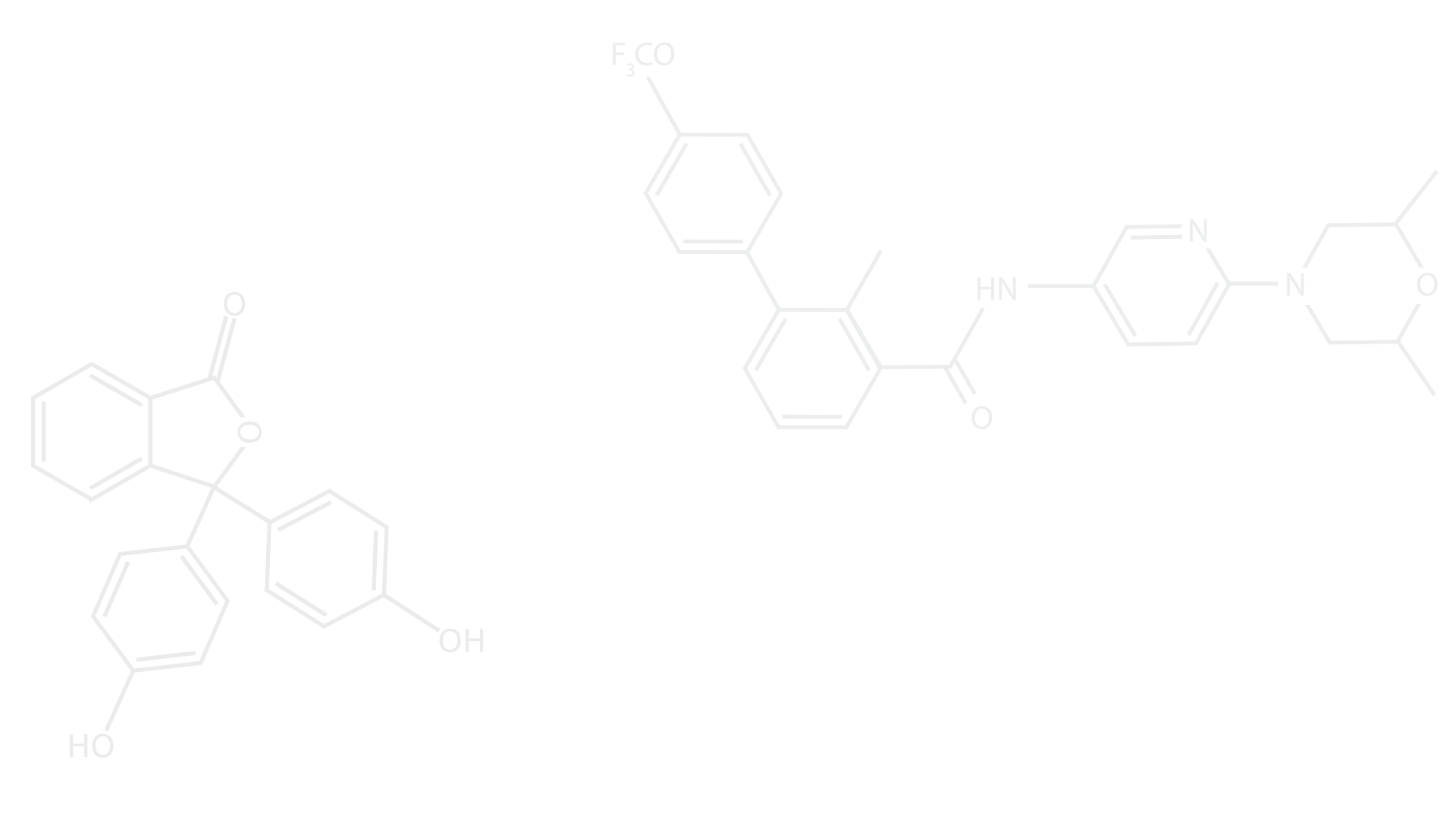
יחד עם חומרי ההדברה ישנם גם "תוספים" שמקנים לחומרים הפעילים יעילויות מסוימות, כגון: שינוי אנרגיית פני השטח והיספחות מקסימלית על-פני המזיק, יכולות ספיחה פנימית אפקטיבית עבור סוגי עשבים מסוימים וכו'. פיתוח ורישוי של חומרי הדברה הוא לא עניין של מה בכך, וזמן הפיתוח, הבדיקה והרישוי, עלול לקחת מס' שנים, בדומה לפיתוח ואישור תרופה. הדבר נובע מכך, שבסופו של יום חומרים אלו נשארים או משתחררים לסביבה, ועלולים להסב נזק - מה שמצריך את בדיקת היעילות והרעילות שלהם בצורה ייחודית וחד-חד ערכית. ישנם חומרי הדברה ששימשו למטרות צבאיות (לא הוגדרו כחומרי הדברה, אלא חומרי לחימה), ועברו הסבה לחומרי הדברה למטרות חקלאות, לדוגמא: חומרים ממשפחת האורגנו-פוספטים (מבנה כימי בתמונה מטה, משמאל) שכיום משמשים כ50% מחומרי ההדברה הקיימים, אשר להם מנגנון דומה לגז עצבים (אינהיביטורים של האנזים אצטיל-כולין-אסטראז). אותו האנזים אחראי לפעילות חשובה מאוד ב"שידור" סיגנלים לגוף מהמוח, ובעצם אחראי לפירוק יעיל של הניורוטרנסמיטור אצטיל-כולין (מתואר בתמונה מטה, מימין). כאשר חומר הדברה ממשפחת האורגנו-פוספטים יוצר קשירה קווולנטית בלתי הפיכה עם אותו האנזים (אצטיל-כולין-אסטראז), הוא גורם לשינוי מבני ומונע ממנו לפרק את האצטיל-כולין - דבר המביא לכמות גדולה יותר של אצטיל-כולין בגוף באופן מסוכן, הגורם להרעלה.
איור יפה שמסביר את המנגנון נמצא מתחת ל2 האיורים של המבנים הכימיים.
קרדיט: https://creativemeddoses.com/topics-list/organophosphate-poisoning/
איך זה קשור למעבדה שלנו?
במעבדה שלנו מפתחים חיישנים ננומטרים חכמים שיכולים לחוש מזהמים אלו בנוזלים, עד לריכוזים של פחות מחלקיק אחד מסוכן למיליארד מולקולות נוזל!
רוצים לקרוא עוד?
או לחצו כאן לכתבה בנושא.



מה מיוחד בצבעי הנוצות של הטווס?
רוב הצבעים המוכרים כיום בטבע נובעים מחומרים הנקראים פיגמנטים. חומרים אלו עובדים על עיקרון של בליעת חלק מהאור הפוגע בהם והחזרת אורך גל מסוים אותו אנחנו רואים. צבעים אלו מופיעים בצמחים ובבעלי החיים השונים, אך ישנם כמה בעלי חיים שצבעיהם מתקבלים בשיטה קצת אחרת, המוכר מביניהם הוא הטווס.
אז איך מתקבלים הגוונים בנוצות?
המדען הנודע רוברט הוק חקר את נוצות הטווס בסוף המאה ה17. הוא השתמש במיקרוסקופ, שרק הומצא כמה שנים קודם לכן, ומצא שבנוצות יש מבנים קטנים. הוא טען שיש למבנים אלו את היכולת ליצור את הצבעים המוכרים לנו. רק 100 שנים לאחר מכן הובן יותר לעומק המושג של צבע מבני.
מהי צבעוניות מבנית?
עבור מבנים קטנים מאוד, ברמה הננומטרית, יכולים להתקבל צבעים שונים על ידי התאבכות בונה והורסת של גלי האור בשכבות החומר. אורך גל שיתאים למבנה יופיע ואילו שאר אורכי הגל ייעלמו.
בנוצות הטווס ואצל בעלי חיים אחרים, ישנו מבנה של חלק בגוף המורכב ממבנה ננומטרי כזה. עובי המבנה והמרווחים בין המבנים הללו יכולים ליצור מגוון רחב של צבעים. כך מתקבל מצב שנוצות הטווס, שבפועל הן בצבע חום, נראות בגוונים של צהוב-ירוק-כחול.
למה מבנים כאלו יכולים לשמש אותנו?
מעבדות האופטיקה השונות מנסות לחקות את המבנים האלה ליצירת מגוון רחב של טכנולוגיות. לדוגמה, ציפויים המסוגלים לשנות את צבעם בתנאים שונים. כמו כן, גם התקני תצוגה והעברת מידע שונים המבוססים על רגישות גבוהה או אפילו חיישנים המשנים את צבעם לפי החומר. טכנולוגיות אלו נחשבות לאמינות ובעלות עמידות גבוהה יותר מאלו הקיימות כיום.


מה הקשר בין כרובית לשלג?
גם לפתית שלג וגם לכרוכית יש מבנה פרקטלי, המאופיין בתכונה הנקראת "דמיון עצמי".
מהו פרקטל?
פרקטל הוא צורה גיאומטרית הדומה לעצמה בכל סקלה שנסתכל בה. כלומר, ככל שנתבונן אל תוך חלקיו של הפרקטל- נמשיך לראות את אותה הצורה והוא תמיד ידמה לצורתו המקורית במידות ההגדלה השונות. תכונה זו של הפרקטל נקראת "דמיון עצמי".
המתמטיקאי גאורג קנטור שחי בסוף המאה ה-19 היה הראשון לבנות פרקטל, אותו כינה "אבק קנטור". אחריו, המתמטיקאי השוודי הלגה פון קוך בנה פרקטל אחר מפורסם המכונה "פתית השלג של קוך". את השם "פרקטל" טבע המתמטיקאי האמריקאי בנואה מנדלברוט בתחילת שנות השישים, אותה גזר מהמילה היוונית FRACTUM שמשמעה שבור, לא רציף.
כיצד בונים פרקטל?
השיטה: לבצע סידרה של פעולות שוב ושוב, בכל פעם ליישם את הכלל על תוצאתו של השלב הקודם.
הכלי: הכלי העיקרי לייצור פרקטלים הוא באמצעות המחשב,אשר מאפשר לבצע מיליוני חזרות של פעולות מתמטיות. לדוגמה, לבניית הפרקטל של מנדלברוט נדרשות 6,000,000 חזרות של פעולות מתמטיות.
פרקטלים בטבע
בטבע ניתן למצוא בטבע פרקטלים רבים: עננים, פתיתי שלג, ברקים, קונכיות, ואף ירק הכרובית שבה כל אחד מהפיצולים הם למעשה כרובית קטנה יותר. דוגמות נוספות הן כלי הדם המסתעפים ומתפצלים שוב ושוב בגופנו, ומבנה הריאות - רשת סבוכה של צינורות המתפצלת לענפים ולענפי משנה, ולה יתרון גדול בכך שהיא מגדילה מאד את שטח הפנים של הריאות ובכך גם את קליטת החמצן המגיע לדם.

למה אסור לטוס אחרי צלילה?
אני מניחה ששמעתם על חנקן שמשתחרר בלחצים נמוכים.
זה נכון, אבל בואו נעשה סדר..
זה מתחיל מחוק הנרי, רופא וכימאי אנגלי שהציע בשנת 1803 משוואה המתארת המסה של גזים בנוזלים. חוק הנרי קשור גם לקורס כימיה פיזיקלית הנלמד במהלך תואר ראשון במחלקה לכימיה בבר-אילן.
אז מה החוק אומר?
בטמפרטורה קבועה, כמות הגז המומס בנוזל (ממס) פרופורציונית ללחץ החלקי של הגז הנמצא בשיווי משקל עם הנוזל.
זה אומר את שני הדברים הבאים:
-
המסיסות של הגז גדלה בנוזל כאשר הלחץ עולה. זאת מכיוון שאז יותר גז נספח בנוזל.
-
כאשר הטמפרטורה עולה המסיסות של הגז בנוזל קטנה. ככל שהנוזל קר יותר - יותר גז נספח, וכשהנוזל מתחמם- הגז בורח.
-
איך אנחנו רואים זאת בחיי היום יום?
נסתכל על סודה – כאשר הבקבוק סגור, באותם תנאי לחץ הפחמן הדו חמצני מומס בתוכו. כאשר אנחנו פותחים את הבקבוק הלחץ יורד ולכן הגז משתחרר.
גם בנביעות באירופה תוכלו לראות תופעה זאת בה המים נובעים עם בועות שמבעבעות.
אז מה קורה בצלילה?
בלחץ גבוה במעמקים (כל 10 מטר זו אטמוספרה), החנקן מומס בדם וברקמות, כאשר הצוללן עולה החנקן מומס פחות ורוצה להשתחרר. אם החנקן משתחרר כבועות גדולות זה יכול לפגוע בתפקוד הפיזיולוגי. לכן גם לא מומלץ לקחת אמבטיה חמה לאחר צלילה או לעשות פעילות אקטיבית.
מה קורה למטפסי הרים?
שם התופעה הפוכה, לחץ החמצן החלקי באוויר יורד. על זה בפעם הבאה...
למה אסור לטוס אחרי צלילה?
אני מניחה ששמעתם על חנקן שמשתחרר בלחצים נמוכים.
זה נכון, אבל בואו נעשה סדר..
זה מתחיל מחוק הנרי, רופא וכימאי אנגלי שהציע בשנת 1803 משוואה המתארת המסה של גזים בנוזלים. חוק הנרי קשור גם לקורס כימיה פיזיקלית הנלמד במהלך תואר ראשון במחלקה לכימיה בבר-אילן.
אז מה החוק אומר?
בטמפרטורה קבועה, כמות הגז המומס בנוזל (ממס) פרופורציונית ללחץ החלקי של הגז הנמצא בשיווי משקל עם הנוזל.
זה אומר את שני הדברים הבאים:
-
המסיסות של הגז גדלה בנוזל כאשר הלחץ עולה. זאת מכיוון שאז יותר גז נספח בנוזל.
-
כאשר הטמפרטורה עולה המסיסות של הגז בנוזל קטנה. ככל שהנוזל קר יותר - יותר גז נספח, וכשהנוזל מתחמם- הגז בורח.
-
איך אנחנו רואים זאת בחיי היום יום?
נסתכל על סודה – כאשר הבקבוק סגור, באותם תנאי לחץ הפחמן הדו חמצני מומס בתוכו. כאשר אנחנו פותחים את הבקבוק הלחץ יורד ולכן הגז משתחרר.
גם בנביעות באירופה תוכלו לראות תופעה זאת בה המים נובעים עם בועות שמבעבעות.
אז מה קורה בצלילה?
בלחץ גבוה במעמקים (כל 10 מטר זו אטמוספרה), החנקן מומס בדם וברקמות, כאשר הצוללן עולה החנקן מומס פחות ורוצה להשתחרר. אם החנקן משתחרר כבועות גדולות זה יכול לפגוע בתפקוד הפיזיולוגי. לכן גם לא מומלץ לקחת אמבטיה חמה לאחר צלילה או לעשות פעילות אקטיבית.
מה קורה למטפסי הרים?
שם התופעה הפוכה, לחץ החמצן החלקי באוויר יורד. על זה בפעם הבאה...
Why is it forbidden to fly after diving?
I assume you know that nitrogen is released at low pressure.
This is true, but let’s sort things out….
It all begins with Henry’s law, an English M.D and chemist who, in 1803, suggested an equation that describes the mass of gasses in liquids. Henry’s law also has to do with the physical-chemistry course given in Chemistry undergraduate studies in Bar-Ilan University.
What does this law mean?
At a constant temperature, the amount of gas solvated in a liquid (solute) is proportional to the partial pressure of the gas that is in equilibrium with the liquid.
This has two implications:
-
The solubility of the gas increases with increasing pressure. Because more gas is adsorbed by the liquid.
-
When the temperature increases the amount of gas in the liquid is reduced. The colder the liquid the more gas is adsorbed, and when the liquid is heated the gas escapes.
How does this affect our lives?
Let’s look at a bottle of soda water. When the bottle is closed under the same pressure the carbon dioxide is solvated in the water. When we open the bottle the pressure is reduced and the gas is released. This can be observed in water spouts in Europe – the water spouts with bubbles.
At high pressure in deep water (every 10 meters is an atmosphere), nitrogen is solvated in our blood and tissue. When the diver rises to the water surface the nitrogen is released. If the nitrogen is released as large bubbles it can damage the body physiology. It is therefore not recommended to have a hot bath or sports activity after diving.
What happens to mountain climbers?
The phenomenon there is exactly the opposite, the partial pressure of oxygen is reduced. We’ll keep that for the next time…

ריח של גשם
האם שאלתם את עצמכם מדוע יש לגשם ריח? או איך אנחנו מריחים את הגשם אפילו לפני שהוא מגיע...
כמו בכל דבר אחר בחיים, גם כאן לכימיה מקום מרכזי.
הריח הוא תוצאה של מולקולה קטנה, geosmin שהיא סוג של כוהל, שאנחנו מצליחים לזהות ברגישות גבוהה ביותר. את המולקולה הזאת מפרישה בקטריה, השוכנת באדמה ובין היתר מפרקת מזון ושיירים.
אז איך זה קורה?
בתקופות של יובש, הבקטריה הזאת פחות פעילה, אך לפני רדת הגשם, כשהלחות עולה, ובמיוחד באדמה אוורירית, הבקטריה מתחילה להיות פעילה יותר וליצר ריח של גשם, זוהי המולקולה שלנו geosmin. כשהגשם יורד, ישתחרר חלק מהאדמה נסחף, והמולקולה שלנו המסיסה למים משתחררת ונישאת ע"י הרוח במורד ההר, מזהירה את האנשים בשכונה ליד שהגשם מגיע.
מה מפתיע אותי?
אנחנו יכולים לזהות את המולקולה הזאת ברגישות של 5 מולקולות לטריליון.
מה אני שואלת?
לגשם ביער ריח שונה מזה של העיר.. למה?
איך זה קשור למעבדה שלנו?
בעזרת אנטנות ננומטריות, אנחנו מפתחים גלאי אור (סנסורים באנגלית) המזהים חומרי הדברה במים ברגישות של 5 מולקולות לביליון. ישנם עוד אתגרים, אבל אלעד סגל, דוקטורנט במעבדה שעובד על זה, כבר זכה במלגה מטעם משרד המדע על הנושא, ועובד כרגע על הקמת מיזם חדש בנושא.

Why can you smell rain?
Have you ever asked yourself, why does the rain have a smell? Or how is it we smell the rain even before it has started?
Like everything in our lives, chemistry plays a role here.
The smell of the rain comes from a small molecule call geosmin. Geosmin is an alcohol that we are very sensitive to. It comes from bacteria that is in the ground and decomposes food and other substances.
How does it happen?
When the weather is dry the bacteria is barely active. It becomes more active when the moisture in the air rises, especially in airy grounds, and starts to release the geosmin molecule, creating the smell of rain.
What a surprise!
Our sensitivity to this molecule is 5 molecules in a billion.
Question:
The smell of rain in a forest is different than that in the town, why?
